ЖЕЛУДОЧНОЕ И ДУОДЕНАЛЬНОЕ СОДЕРЖИМОЕ
Желудочное и дуоденальное содержимое.
Желудочный сок — продукт внешнесекреторной и экскреторной деятельности желез желудка, имеет сложный неорганический (вода, соляная кислота, хлориды, сульфаты, фосфаты, бикарбонаты, аммиак, натрий, калий, кальций, магний, водород) и органический (представлен веществами белковой и небелковой природы) состав, отличаясь от других пищеварительных секретов выраженной кислой реакцией, особенностями ферментов и высокомолекулярных соединений. Объем и состав его варьируют в зависимости от соотношения нервных и гуморальных факторов, вида и силы раздражителя, видовых и возрастных особенностей, давления в полости желудка.
В сутки у человека выделяется около 2–2,5 л сока — бесцветной жидкости (относительная плотность 1,002–1,007) без запаха. Его цвет и свойства меняются от присутствия слюны, желчи, крови, панкреатического и кишечного соков. При низкой кислотности и нарушении эвакуации он может приобрести запах за счет остатков забродившей пищи. Желудочный сок обладает выраженным бактерицидным и бактериостатическим свойствами, в происхождении которых ведущее значение имеет соляная кислота (HCl). Отличается также зависимость степени бактерицидности нейтрального или слабощелочного сока от интенсивности желудочного лейкопедеза. Основным энзиматическим процессом в полости желудка является начальный гидролиз белков. В клинической практике чаще всего проводятся лабораторные диагностические исследования желудочного содержимого с определением в нем: показателей кислотной секреции и активности ферментов; показателей цитопротекции; микробной флоры желудка.
Методы функционального исследования секреции желудка можно разделить на две группы:
1. Зондовые:
аспирационный, фракционный;
внутрижелудочной перфузии;
внутрижелудочного титрования;
внутрижелудочной рН-метрии.
2. Беззондовые:
проба с метиленовым синим (проба Сали);
исследования с применением ионообменных смол;
ацидотест;
определение уропепсина;
метод радиотелеметрии;
определение секреции с помощью индикатора конго красного;
тест с азуром А;
определение сывороточных пепсиногенов I группы.
Беззондовые методы в настоящее время применяются редко, поскольку существуют более информативные, безопасные и простые методы, такие как аспирационный, фракционный с пентагастриновой стимуляцией и внутрижелудочной рН-метрии. Исследования кислотопродуцирующей функции желудка в клинике стали возможны после предложения для зондирования желудка специального зонда и стимуляторов секреции соляной кислоты. Первоначально предлагались энтеральные пробные завтраки: мясной бульон; капустный сок; раствор кофеина.
Однако получаемые различными исследователями результаты значительно отличались друг от друга, что в конечном итоге заставило отказаться от применения этих пробных завтраков. Было открыто стимулирующее действие гистамина на секреторную функцию желудка. В настоящее время в клинической практике широко распространены субмаксимальный гистаминовый тест (0,008 мг/кг гистамина гидрохлорида подкожно) и более информативный максимальный гистаминовый тест (0,025 мг/кг гистамина гидрохлорида подкожно). Недостатком гистамина является возможность возникновения побочных эффектов (сосудистых реакций). Максимальная секреторная реакция желудка отмечается и при подкожном введении 6 мкг/кг С-концевого тетрапептида гастрина-пентагастрина, который практически не вызывает побочных реакций.
Аспирационный фракционный метод зондирования желудка. Фракционное аспирационное исследование секреции желудка в настоящее время проводится практически однотипно во всех клинических лабораториях и ориентировано на интегральный показатель — выработку соляной кислоты в единицу времени с учетом объема секреции.
Принцип зондирования. Получение чистого желудочного секрета путем активной аспирации на различных этапах секреторной деятельности желудка. Оборудование:
Тонкий зонд (полая резиновая трубка диаметром 4–5 мм, длиной около 1,5 м с метками на расстоянии 50–55 см и 70–75 см от слепого конца зонда).
Пробирки.
Штативы для пробирок.
Лоток.
Воронка.
Шприц вместимостью 20 мл, или водоструйный насос стандартной конструкции, или аспирационный вакуум-отсос.
Один из активных стимуляторов желудочной секреции.
Ход зондирования. Зондирование лучше проводить в специальном помещении. Перед исследованием секреторной функции желудка необходимо отменить медикаментозные препараты не менее чем за 24 часа до исследования и проводить его обычно утром после 14-часового голодания. Конец тонкого зонда помещают в глубине глотки на корень языка и предлагают сделать несколько неторопливых глотательных движений, благодаря чему зонд продвигается по пищеводу. Введение зонда до первой метки свидетельствует о том, что внутренний конец его находится в области дна желудка, а продвижение зонда до второй метки указывает на то, что он достиг привратника желудка. Необходимым условием полного извлечения желудочного содержимого является введение зонда на глубину, рассчитанную следующим образом: рост пациента в сантиметрах минус 100.
После введения зонда полностью извлекают содержимое желудка натощак, что составляет отдельную порцию для исследования. Затем в течение часа собирают секрет желудка, выделяющийся в результате стимулирующего влияния зонда и аспирации — базальная секреция (basal acid output, или ВАО). Потом начинают активную стимуляцию работы слизистой оболочки желудка введением энтерального или парентерального стимулятора, после чего желудочный сок собирают также в течение часа — стимулированная, или максимальная секреция (maximal acid output, или МАО). Аспирацию базального и стимулированного сока проводят в течение каждых 15 минут первого и второго часа зондирования. Таким образом, за каждый час получают 4 порции желудочного сока, которые составляют так называемое часовое напряжение соответствующего периода желудочной секреции. Полученные порции желудочного сока подвергают физико-химическому исследованию. Всего исследуют 9 порций: порция, полученная натощак, затем 4 порции в течение каждых 15 минут первого часа зондирования и 4 порции в течение второго часа зондирования.
Исследование желудочного сока включает определение физических свойств, химическое и микроскопическое исследование.
Физические свойства. Количество. Измеряют каждую порцию желудочного сока и высчитывают его объем во все фазы секреторного цикла. Объем сока натощак не должен превышать 50 мл, в условиях базальной секреции объем сока за час может быть 50–100 мл, в фазе стимулированной секреции в ответ на пищевой раздражитель — 50–110 мл, на субмаксимальную стимуляцию гистамином 100–140 мл. Часовой объем желудочного сока в ответ на стимуляцию с применением максимальных доз гистамина по Кею составляет 180–220 мл.
Запах. У нормального желудочного содержимого запах отсутствует либо слегка кисловатый. При снижении содержания соляной кислоты или полном ее отсутствии желудочное содержимое приобретает своеобразный запах масляной, молочной или уксусной кислоты за счет образующихся продуктов брожения. Если в желудке развиваются гнилостные процессы вследствие гниения белка или распада раковой опухоли, желудочный сок приобретает гнилостный запах. Гнилостный запах может свидетельствовать и о нарушении эвакуации из желудка.
Цвет. Нормальное желудочное содержимое бесцветно. В присутствии желчи при ахилии, оно имеет желтый цвет, при наличии соляной кислоты — зеленый за счет того, что в кислой среде билирубин желчи окисляется в биливердин. Изменяется окраска желудочного содержимого и в присутствии крови. Под влиянием соляной кислоты гемоглобин крови превращается в солянокислый гематин, придавая желудочному содержимому более или менее интенсивную коричневую окраску. При отсутствии в желудочном содержимом соляной кислоты цвет его при примеси крови красный. Интенсивность окраски зависит от степени кровотечения.
Слизь. В норме присутствует в желудочном соке в небольшом количестве. Увеличение содержания слизи наблюдается при гастрите и других поражениях слизистой оболочки желудка. Слизь, плавающая на поверхности желудочного сока, представляет собой слюну, мокроту либо содержимое носовой части глотки, она насыщена воздухом, легкая, в виде грубых хлопьев и комков, диагностического значения не имеет.
Примеси. Остатки пищевых масс, которые могут быть обнаружены, говорят о нарушении эвакуации из желудка.
Химическое исследование. Химическое исследование желудочного содержимого дает возможность получить представление о кислото-, ферменто-, белковообразующей и других функциях желудка.
Исследование кислотообразующей функции желудка. Общая кислотность желудочного сока состоит из трех кислых валентностей: свободной (диссоциированной) соляной кислоты, связанной соляной кислоты и кислотного остатка. Под свободной кислотностью, концентрацией ионов водорода [Н+], следует понимать концентрацию свободной, полностью диссоциированной соляной кислоты.
Под связанной кислотностью следует понимать концентрацию ионов водорода, связанных карбоксильными группами белков и пептидов. В состав кислотного остатка входят органические кислоты (масляная, молочная, уксусная) и кислореагирующие фосфаты. Наиболее распространенный способ измерения кислотности желудочного сока — титрование его сильной щелочью (0,1 н раствор NaOH) в присутствии индикаторов, меняющих окраску в зависимости от рН среды.
Для определения общей кислотности желудочного сока применяется индикатор фенолфталеин, который в кислой среде остается бесцветным, а в щелочной, при рН 8,2–10,0, приобретает розовый цвет. Индикатор диметиламиноазобензол оранжевого цвета в присутствии свободной соляной кислоты при рН 2,4–4,0 становится красным, а при отсутствии ее — оранжевым или желтым. Индикатор ализаринсульфоновокислый натр, имеющий вишневую окраску, в кислой среде приобретает желтый цвет, а в зоне рН 4,3–6,3 — фиолетовый. В присутствии этого индикатора оттитровываются свободная соляная кислота и кислотный остаток желудочного содержимого.
Если индикатор диметиламиноазобензол при добавлении к желудочному соку изменяет свой цвет на красный, для титрования применяют метод Михаэлиса. Если диметиламиноазобензол меняет свою окраску на желтую, желудочный сок необходимо титровать по методу Тепфера. При определении кислотности желудочного сока титрационными методами нужно строго следить за изменением окраски в стаканчиках и точно отмечать уровень щелочи в бюретке.
Метод Михаэлиса. Реактивы: 1%-й спиртовой раствор фенолфталеина, 0,5%-й спиртовый раствор диметиламиноазобензола, 0,1 н раствор едкого натра.
Посуда и оборудование. Бюретки емкостью 25, 50 или 100 мл, штатив Бунзена, химические стаканчики емкостью 50 мл, воронки, пипетки градуированные емкостью 5 мл или 10 мл.
Ход исследования. В химический стакан отмеривают 5 мл профильтрованного через 2 слоя марли желудочного сока, затем вносят 1–3 капли раствора диметиламиноазобензола и 1–2 капли раствора фенолфталеина. Титруют 0,1 н. раствором едкого натра при постоянном помешивании. Предварительно отмечают уровень 0,1 н раствора едкого натра в бюретке (I уровень).
Определяют следующие величины:
количество щелочи, израсходованное на титрование желудочного сока от первоначального красного цвета до оранжевого (II уровень);
количество щелочи, израсходованное на титрование от оранжевого до лимонно-желтого (III уровень);
количество щелочи, затраченное на титрование от красного до стойкого розового цвета (IV уровень).
Расчет. Количество щелочи, пошедшей на титрование до первого изменения окраски (разница между II и I уровнем), определяет концентрацию свободной HCl в желудочном соке. Количество щелочи, пошедшей на все титрование, от красной окраски диметиламиноазобензола в резко кислой среде до красной окраски фенолфталеина в щелочной среде, т. е. разница между IV и I уровнем, соответствует общей кислотности. Количество щелочи, пошедшей на титрование до уровня, означающего среднее арифметическое между III и IV уровнем, соответствует концентрации всей HCl (т. е. сумме свободной и связанной), а концентрацию связанной HCl находят по разности между всей HCl и свободной HCl. Разность между общей кислотностью и всей HCl называют кислотным остатком. Таким образом, все кислореагирующие вещества определяют в одной порции.
Пример расчета. Уровень I в бюретке — 4, уровень II — 5,4 (желто-оранжевая окраска), уровень III — 6 (лимонно-желтый цвет), уровень IV — 6,8 (стойкий розовый). Среднее арифметическое между III и IV уровнем — 6,4. Для титрования было взято 5 мл желудочного сока, расчет ведется на 100 мл, поэтому количество щелочи, потраченной на разных этапах титрования, умножают на 20 (если титруют 10 мл желудочного сока, то умножают соответственно на 10).
Свободная HCl: 5,4–4=1,4х20=28
Общая кислотность: 6,8–4=2,8х20=56
Сумма свободной и связанной HCl: 6,4–4=2х20=48
Связанная HCl: 48–28=20
Кислотный остаток: 56–48=8
Унифицированное определение кислотности методом Тепфера. Реактивы:
1%-й спиртовый раствор фенолфталеина. Интервал перехода окраски при рН 8,2–10,0.
0,5% спиртовый раствор диметиламиноазобензола. Интервал перехода окраски при рН 2,9–4,0.
1%-й водный раствор ализаринсульфоновокислого натра. Интервал перехода окраски при рН 4,3–6,3.
0,1 н раствор едкого натра.
Ход исследования. В 2 стакана отмеривают по 5 мл профильтрованного желудочного сока. В первую порцию вносят по 2 капли диметиламиноазобензола и фенолфталеина и определяют концентрацию свободной HCl и общую кислотность. Во вторую порцию желудочного сока прибавляют каплю ализаринсульфоновокислого натра и титруют до перехода желтой окраски в слабо-фиолетовую. В зоне перехода этого индикатора нейтрализуются кислореагирующие вещества, кроме связанной HCl, которую находят по разности между объемом щелочи, пошедшей на нейтрализацию всех кислых валентностей желудочного сока (титрование с фенолфталеином), и объемом, пошедшим на титрование с ализаринсульфоновокислым натром. Все полученные величины умножают на 20 для перерасчета на 100 мл желудочного сока.
В тех случаях, когда объем полученного желудочного сока небольшой, применяют микрохимический способ определения кислотности. Оборудование. Микробюретка. Реактивы те же, что и для метода Михаэлиса.
Ход исследования. В стакан для титрования помещают 1 мл профильтрованного сока и 5 мл дистиллированной воды. Титруя из микробюретки, определяют концентрацию свободной HCl и общую кислотность по методу Михаэлиса.
Расчет. Содержание свободной HCl равно количеству щелочи, пошедшей на титрование до желто-оранжевой окраски (цвет семги) диметиламиноазобензола, умноженному на 100. Общей кислотности соответствует количество щелочи, пошедшей на все титрование, уменьшенное на 0,05 (индикаторная поправка) и умноженное на 100. При низкой кислотности индикаторная поправка должна быть равна 0,03.
Способы выражения кислотности. Традиционным способом выражения кислотности желудочного сока являются титрационные единицы (ТЕ) — объем 0,1 н едкого натра, необходимый для нейтрализации кислых валентностей в 100 мл желудочного сока. Последние годы концентрацию HCl в желудочном соке более принято выражать в миллимолях на 1 л желудочного сока. Известно, что 1 мл 0,1 н раствора едкого натра эквивалентен 1 мл 0,1 н раствора HCl (1 ТЕ), или 0,1 ммоль HCl, отсюда концентрация HCl в 100 мл сока, выраженная в миллимолях HCl, в 10 раз меньше, чем в титрационных единицах.
Пример. Если концентрация HCl 40 ТЕ, то это соответствует концентрации 4 ммоль в 100 мл сока, или 40 ммоль в 1 л сока. Таким образом, числовое значение концентрации HCl, выраженное в титрационных единицах, совпадает с числовым значением концентрации HCl, выраженным в миллимолях на 1 л (40 ТЕ=40 ммоль/л HCl).
Дебит соляной кислоты. Этот показатель отражает общее количество соляной кислоты, выделенной желудком за определенный отрезок времени. Обычно дебит определяется за 1 час и выражается в миллимолях (1 ммоль = 36,5 мг соляной кислоты).
Различают: Дебит свободной HCl; Связанной HCl. HCl (кислотная продукция). Последний показатель определяют, исходя из цифр общей кислотности. Дебит-час определяют только при условии получения всего желудочного содержимого за час. Величину кислотовыделения вычисляют по двум формулам, которые несколько отличаются друг от друга в зависимости от выражения дебита (в миллиграммах или в миллимолях) HCl.
Для расчета дебита HCl в миллиграммах применяют следующую формулу: D=V1 х E1 х 0,0365+V2 х E2 х 0,0365+..., где D — дебит HCl (мг); V — объем порции желудочного сока (мл); Е — концентрация HCl (ТЕ); 0,0365 — количество миллиграммов HCl в 1 мл сока при концентрации ее, равной 1 ТЕ.
Число слагаемых определяется числом порций за время исследования. Для расчета дебита HCl в миллимолях (для HCl эти величины совпадают) применяют другую формулу: D = ((V1 х E1)/1000)+((V2 х E2)/1000)+ ..., где D — дебит HCl (ммоль), а остальные обозначения те же, что и в предыдущей формуле.
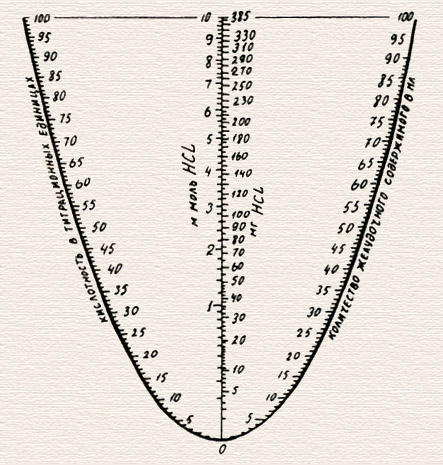
Номограмма для определения дебита соляной кислоты.
Для облегчения подсчета дебит-часа HCl можно пользоваться номограммой. Линейкой соединяют нанесенные на противоположных ветвях кривой цифры, соответствующие объему и кислотности данной порции желудочного сока. В месте пересечения линейки с вертикальной линией находят значение дебита, выраженное в миллиграммах HCl или в миллимолях HCl.
Нормальные показатели кислотности. Базальная секреция.
Часовой объем — 50–100 мл
Общая кислотность — 40–60 ммоль/л
Свободная соляная кислота — 20–40 ммоль/л
Связанная соляная кислота — 10–20 ммоль/л
Кислотный остаток — 2–8 ммоль/л
Дебит-час HCl — 1,5–5,5 ммоль/ч
Дебит-час свободной HCl — 1,0–4,0 ммоль/ч
Секреторная реакция желудка на пищевые пробные раздражители
Часовой объем — 50–110 мл
Общая кислотность — 40–60 ммоль/л
Свободная HCl — 20–40 ммоль/л
Связанная HCl — 10–20 ммоль/л
Кислотный остаток — 2–8 ммоль/л
Дебит-час HCl — 1,5–6,0 ммоль/ч
Дебит-час свободной HCl — 1,0–4,5 ммоль/ч
Секреторная реакция желудка на субмаксимальную гистаминовую стимуляцию.
Часовой объем — 100–140 мл
Общая кислотность — 80–100 ммоль/л
Свободная HCl — 65–85 ммоль/л
Связанная HCl — 12–23 ммоль/л
Кислотный остаток — 3,0–12 ммоль/л
Дебит-час HCl — 8,0–14,0 ммоль/ч
Дебит-час свободной HCl — 6,5–14,0 ммоль/ч
Секреторная реакция желудка на максимальную гистаминовую стимуляцию.
Часовой объем — 180–220 мл
Общая кислотность — 100–120 ммоль/л
Свободная HCl — 90–110 ммоль/л
Связанная HCl — 10–15 ммоль/л
Дебит-час HCl — 18–26 ммоль/ч
Дебит-час свободной HCl — 16–24 ммоль/ч
Метод внутрижелудочной перфузии. Одним из существенных недостатков аспирационного фракционного метода является невозможность аспирации сока. При соблюдении всех правил исследования удается получить не более 46,3–85% секретированного желудочного сока. В связи с этим предложен метод внутрижелудочной перфузии. Принцип метода основан на определении полноты аспирации каждой порции желудочного сока и вычислении величины кислотопродукции с учетом количества неаспирированного секрета.
Метод внутрижелудочного титрования. Аспирационные методы исключают такой важный компонент секреторной реакции на прием пищи, как растяжение желудка. Для исключения этого фактора был разработан способ внутрижелудочного титрования. Принцип метода заключается в титровании продуцируемой желудком кислоты щелочью непосредственно в полости желудка. Внутрижелудочное титрование используется для изучения секреторной реакции желудка на прием пищи или каких-либо ее ингредиентов.
Внутрижелудочная рН-метрия. В клинической практике активно применяется такой метод исследования кислотообразующей функции желудка, как внутрижелудочная рН-метрия с использованием оригинальных одно-, двух- и трехоливных рН-зондов конструкции Е.Ю. Линара. Преимуществом рН-метрии является возможность непрерывной одновременной регистрации рН в теле, антральном отделе желудка и в двенадцатиперстной кишке в условиях базальной и стимулированной (гистамином) желудочной секреции.
Беззондовые методы исследования желудочной секреции. Проба Сали. Основана на том, что только желудочный сок, содержащий соляную кислоту и пепсин, способен переваривать соединительную ткань (кетгут).
На небольшой кусочек кондомной резины высыпают 0,1 г метиленового синего, резину перевязывают распаренным кетгутом №5. Мешочек отмывают от остатков метиленового синего, попавшего на его поверхность, а затем повторно погружают в стаканчик с чистой водой для проверки герметизации. Если вода не окрашивается в синий цвет, мешочек завязан правильно и готов к употреблению.
Методика. Больной проглатывает натощак десмоидный мешочек, затем съедает завтрак. Через 3,5 и 20 часов после этого собирают три порции мочи. Определяют время и интенсивность окраски мочи метиленовым синим.
Оценка результатов. При гиперацидном состоянии окрашены все три порции мочи, причем 2-я и 3-я — в интенсивно синий цвет; при нормальной секреции 1-я порция не окрашена, 2-я окрашена в бледно-зеленый цвет; 3-я окрашена более интенсивно. Незначительное окрашивание только 3-й порции мочи наблюдается при гипоацидном состоянии.
Анацидное состояние характеризуется отсутствием окраски во всех трех порциях мочи больного. Если желудочное содержимое резко кислое (рН 1,5 и ниже), окраска мочи тоже отсутствует. Пепсиноген превращается в пепсин при рН 1,5–3. Если рН желудочного сока менее 1,5, в нем содержится только пепсиноген, который не способен к процессу переваривания. При получении по десмоидной пробе анацидного состояния рекомендуется повторить исследование, дав проглотить больному десмоидный мешочек после еды, т. е. на высоте желудочной секреции.
Проба с ацидотестом. Ацидотест состоит из таблеток кофеин-бензоата натрия и тест-драже (ВНР). Можно заменить таблетки кофеин-бензоата натрия в тесте контрольным завтраком. Состав завтрака: каша рисовая, 100 г мяса, 150 г хлеба, стакан чая.
Методика. После контрольного завтрака больному дают проглотить тест-драже, предварительно собрав его мочу в бутыль (контрольная моча). Через 1,5 часа снова собирают мочу и обе бутыли направляют в лабораторию. Контрольную и вторую порции мочи разбавляют водой до 200 мл; из каждой разбавленной порции наливают в пробирку 5 мл мочи, куда затем добавляют 5 мл 25%-й соляной кислоты.
Оценка результатов. Если в желудочном соке содержится свободная соляная кислота, то во второй пробирке появляется алое или розовое окрашивание. Ориентировочно кислотность желудочного сока можно определить по интенсивности окраски мочи во второй пробирке. Окраску в пробирке сравнивают с окраской колориметрической шкалы, приложенной к ацидотесту.
Унифицированный метод Туголукова. Принцип. Определение протеолитической активности желудочного сока по количеству расщепленного белка. Реактивы: 2%-й раствор сухой плазмы на 0,1 н растворе HCl. 10%-й раствор трихлоруксусной кислоты.
Оборудование.
Центрифужные пробирки (точно градуированные).
Пробирки химические.
Пипетки вместимостью 1, 2 и 10 мл.
Микропипетки вместимостью 0,1 мл.
Центрифуга.
Термостат.
Ход исследования. Желудочный сок, профильтрованный через бумажный фильтр, разводят в 100 раз (9,9 мл воды и 0,1 мл желудочного сока, отмеренного микропипеткой). В одну градуированную центрифужную пробирку помещают 1 мл разведенного сока (опыт), в другую — 1 мл предварительно прокипяченного разведенного сока (контроль). В обе пробирки добавляют по 2 мл 2%-го раствора сухой плазмы и ставят их в термостат при 37°С на 20 час. По прошествии этого времени в каждую пробирку приливают по 2 мл 10%-й трихлоруксуной кислоты, перемешивают стеклянной палочкой до однородной суспензии и центрифугируют 10 минут при 1500 об/мин.
Расчет. По разнице величин осадка в контроле и опыте определяют степень переваривания белка с последующим перерасчетом на количество пепсина. Показатель переваривания субстрата вычисляют по формуле: M = (A–B) x (40/A), где М — показатель переваривания; А — объем осадка в контроле; В — объем осадка в опыте; 40 — постоянная величина, установленная экспериментальным путем.
Совместно с Мегаэнциклопедией «Кирилла и Мефодия»
| официальный сайт © ООО «КМ онлайн», 1999-2026 | О проекте ·Все проекты ·Выходные данные ·Контакты ·Реклама | |||
|
|
Сетевое издание KM.RU. Свидетельство о регистрации Эл № ФС 77 – 41842. Мнения авторов опубликованных материалов могут не совпадать с позицией редакции. Мультипортал KM.RU: актуальные новости, авторские материалы, блоги и комментарии, фото- и видеорепортажи, почта, энциклопедии, погода, доллар, евро, рефераты, телепрограмма, развлечения. Подписывайтесь на наш Telegram-канал и будьте в курсе последних событий.
|







Комментарии читателей Оставить комментарий